Probablemente nunca escoitou falar de Katalin Karikó, pero grazas a ela temos as vacinas de ARN mensaxeiro (ARNm) contra a Covid-19 (producidas por Moderna e Pfizer- BioNTech). Sen a perseveranza desta científica, miles de millóns de doses non estarían administradas a día de hoxe. Como pode imaxinar, chegar ata este punto non foi un camiño sinxelo.
Todo comezou en 1955, cando Katalin Karikó naceu na cidade húngara de nome impronunciable: Kisújszállás. Na súa infancia as condicións económicas foron complicadas. Na década dos 50 do século pasado Hungría aínda sentía a devastación trala Segunda Guerra Mundial mentres a ocupación soviética controlaba o país.
Karikó e a súa familia vivían nunha casa de adobe sen electricidade nin auga corrente. Á investigadora parece non importarlle: “Tiven unha infancia feliz, tiñamos comida sobre a mesa e unha familia amorosa”, aseguraba este ano á revista Lifestyle Magazine. A pesar das carencias, completou os seus estudos e obtivo o seu doutoramento na Universidade de Szeged, onde traballou como bolseira posdoutoral.
Un novo comezo
Despois de formar unha familia e de que o laboratorio no que traballaba quedase sen fondos, Karikó decidiu mudarse a Estados Unidos nos anos 80. Para cumprir o seu soño tivo que vender o seu vehículo (polo equivalente a 1000 dólares) e ocultar o diñeiro dentro dun peluche da súa filla, xa que non se permitía saír do país con máis de 100 dólares.
Chegou a Estados Unidos cunha idea de investigación que nunca abandonaría: o uso da molécula de ARN mensaxeiro con fins terapéuticos. O ARN mensaxeiro é o ácido nucleico que leva a información para producir proteínas con axuda da maquinaria celular. Son as instrucións que indican os compoñentes e orde das proteínas. Esta mensaxe está escrita coas letras que representan a adenina (A), o uracilo (U), a citosina (C) e a guanina (G).
O ARN é unha molécula inestable e fráxil. Ironicamente, así foron os primeiros anos de Katalin Karikó en Estados Unidos, pero ela nunca foi fráxil. Entre 1985 e 1988 traballou na Universidade Temple como investigadora posdoctoral. De 1988 a 1989, na Universidade de Servizos Uniformados de Ciencias da Saúde. En 1989 comezou a traballar como profesora e investigadora na Universidade de Pensilvania. Alí buscou financiamento para as súas investigacións, pero non a obtivo.
Ninguén confiaba no potencial do ARN mensaxeiro.
Debido á falta de diñeiro, a Universidade de Pensilvania non renovou o seu contrato en 1995. A pesar disto, aceptou regresar á posición de investigadora posdoutoral sen a disposición dun laboratorio propio.
En 1995, Katalik Karikó quedou sen contrato e apenas ninguén confiaba no potencial do ARNm
Un encontro fortuíto
Antes da internet, as revistas que publican os artigos científicos chegaban aos institutos, onde tiñan que ser fotocopiadas para ser lidas por todos os investigadores. Xusto no cuarto da fotocopiadora foi onde Karikó coñeceu a Drew Weissman. Intercambiaron un par de frases sobre as súas liñas de investigación e acordaron comezar unha colaboración académica.
Foi o inicio dunha interacción que cambiaría a vida destes científicos.
En 1998 comezaron a realizar experimentos xuntos. Weissman era experto en células dendríticas, que capturan moléculas de microbios e as presentan a outras células do sistema inmunitario para establecer unha mellor defensa. Karikó, na produción in vitro de moléculas de ARN.
O obxectivo era moi claro. No canto de inxectar o virus inactivado ou atenuado, introducirían o ARN mensaxeiro coas instrucións para que, durante un breve tempo, as células do rato producisen unha proteína do virus. Ao entrar en contacto coa devandita proteína, o sistema inmunitario do rato activaríase de maneira moi similar a se estivese infectado co virus real.
Os primeiros resultados foron desalentadores. “O que observamos foi que a pelame dos ratos alterouse, debilitábanse, deixaron de comer e correr. Resultou que o sistema inmunitario recoñece aos microorganismos invasores detectando o seu ARN mensaxeiro e respondendo con inflamación”, lembran Karikó e Weismann.
Ata 2017 documentáronse 214 especies de virus de ARN que infectasen humanos. O sistema inmunitario é moi sensible ao ARN exóxeno –non propio da célula–, xa que pode significar unha infección viral. O mesmo sistema está presente en ratos.
Katalin Karikó preguntábase: “(Se) cada célula do noso corpo (ou dos ratos) produce ARN mensaxeiro e o sistema inmunitario finxe non velo. Que fai diferente ao que eu fixen?”, comentou nun artigo publicado en The New York Times.
Comezaron a estudar como evitar a resposta inflamatoria. Para iso probaron con outros tipos de ARN presentes en mamíferos e atoparon que non todos os tipos de ARN xeraban a mesma reacción. Particularmente o ARN de transferencia (ARNt), unha molécula que actúa como adaptador entre a mensaxe que leva o ARNm e os aminoácidos cos que se forman as proteínas na célula, non activaba as células dendríticas.
Así enganaron ao sistema inmunitario
Os resultados obtidos co ARN de transferencia e o profundo coñecemento de Karikó sobre a química do ARN deulle a idea de modificar os bloques do ARN mensaxeiro. Buscaba preservar o mensaxe pero sen ser recoñecido polo noso corpo como ARN exóxeno. Realizar un cambio silencioso.
Karikó realizou este cambio na uridina (uracilo, unha das letras do ARN, unido a unha molécula de azucre), por unha molécula que presenta un sutil cambio na configuración dos seus átomos, a pseudouridina (Fig 1).
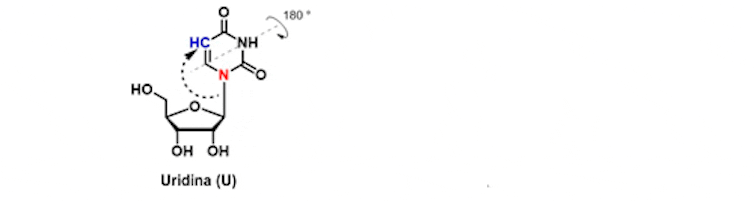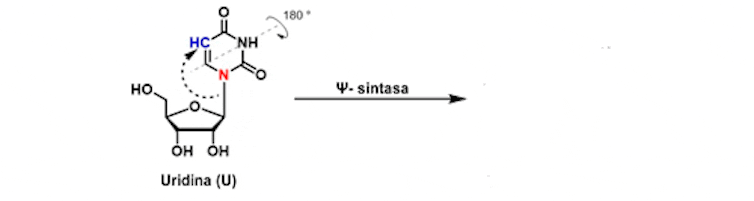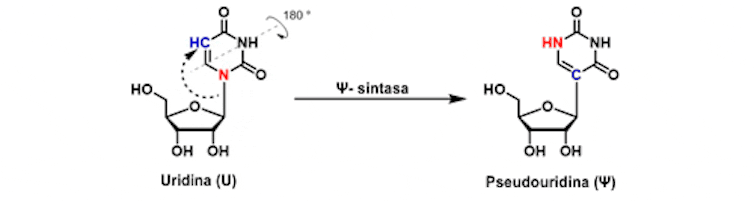
En 2005 Karikó e Weissman mostraron que a modificación de pseudouridina por uridina permite que o ARN mensaxeiro cumpra a súa función ao producir unha proteína desexada pero sen activar as células dendríticas. Lograron enganar ao sistema inmunitario.
Despois de ser rexeitados en múltiples ocasións, publicaron os seus resultados na revista Immunity. Este descubrimento innovador pasou inadvertido para a maioría dos científicos, quen non recoñeceron o valor terapéutico desta modificación.
Un resultado inesperado para Weissman, quen entón prognosticou a Karikó: “O teléfono soará ata que alguén o descolgue, a xente pediranos axuda co ARN. Seremos convidados a dar charlas”. Non ocorreu nese momento.
Ao cabo dos anos, o mundo caería na conta do potencial terapéutico do ARN mensaxeiro.
Con traballos posteriores, Karikó e Weissman lograron demostrar que a incorporación de pseudouridina no ARN mensaxeiro non só reducía a súa capacidade de activar o sistema inmunitario, senón que incrementaba a cantidade de proteína producida.
O desenvolvemento clínico de vacinas de ARN mensaxeiro era cuestión de tempo. Cando a humanidade tivo que enfrontarse á Covid-19, foi un ingrediente primordial da vacina. Todas as uridinas nas vacinas de Moderna e de Pfizer-BioNTech están substituídas por pseudouridinas.
Futuro esperanzador
A técnica do ARN mensaxeiro para xerar vacinas demostrou ser unha excelente ferramenta, grazas ao seu rápido desenvolvemento e a súa alta eficacia. Lembremos que a vacina de Moderna foi deseñada en dous días e obtida en catro semanas.
Para poñer eses datos en perspectiva, no caso da vacina contra a tuberculose, Calmette e Guerín investiron 13 anos para desenvolver o seu famoso bacilo atenuado (BCG). A rapidez no desenvolvemento tamén favorece o deseño de novas vacinas en contra das distintas variantes dos virus.
A día de hoxe iniciáronse polo menos 140 ensaios clínicos utilizando a técnica do ARN mensaxeiro para combater enfermidades infecciosas. No caso particular de vacinas, están en marcha probas contra o zika, VIH, dengue e cancro.
Tan prometedores foron os resultados que, a pesar de que este ano se logrou obter unha vacina suficientemente efectiva en contra da malaria, a compañía BioNTech anunciou que a finais de 2022 iniciará os ensaios clínicos dunha vacina de ARN mensaxeiro contra esta enfermidade.
Hoxe en día é moi fácil albiscar o potencial que ten a molécula de ARN mensaxeiro. Con todo, durante décadas Katalin Karikó recibiu unha negativa tras outra para financiar os seus experimentos. Pero, grazas á súa perseveranza, a súa mente crítica e a súa paixón pola ciencia, logrou cambiar o paradigma e colocar os reflectores sobre o ARN mensaxeiro. Actualmente xa acumulou bastantes premios, entre eles o Premio Princesa de Asturias. Nalgún momento será galardoada co premio Nobel?
* Kevin Navarrete é investigador no laboratorio de Bioloxía Molecular de bacterias patóxenas no Instituto de Microbioloxía de Praga, da Academia Checa de Ciencias; e Yersain Ely Keller de la Rosa é maestro en Ciencias Bioquimicas da Universidad Nacional Autónoma de México (UNAM).
Cláusula de divulgación: as persoas asinantes non reciben salarios, nin exercen labores de consultoría, nin posúen accións, nin reciben financiamento de ningunha compañía ou organización que poida obter beneficio deste artigo, e declararon carecer de vínculos relevantes alén del puesto académico citado.















