A cidadanía española comezará a recibir nas vindeiras semanas a segunda das vacinas contra a Covid-19 aprobadas na Unión Europea. Despois de iniciar a inmunización coa de Pfizer e BioNTech, das que xa se entregaron preto de 800.000 doses e se administraron máis de 150.000 nas comunidades autónomas, a vacina de Moderna comezará a chegar ao país nos vinderos 7 a 10 días. Así o anunciou na mañá do xoves o ministro de Sanidad, Salvador Illa, que estimou que en seis semanas se recibirán 600.000 doses do antídoto, que como a de Pfizer-BioNTech, require de dúas doses para inmunizar a cada persoa que a recibe.
Que se aprobou este mércores?
A Axencia Europea do Medicamento (EMA), despois dun proceso de avaliación que xa leva en marcha varios meses, a medida que se ían recibindo os datos dos ensaios clínicos en marcha coa vacina de Moderna, ofreceu este mércores unha recomendación favorable sobre a eficacia, seguridade e calidade do antídoto desenvolvido pola compañía estadounidense.
Desde que o pasado 30 de novembro, Moderna presentou a solicitude de autorización de comercialización á EMA, realizouse unha supervisión de todos os datos dos ensaios clínicos, e despois de todo este proceso, o Comité de Medicamentos de Uso Humano (CMHP) da EMA recomendou por consenso a autorización condicional de comercialización (ACC), un mecanismo regulamentario que ten a UE para facilitar o acceso temperán a fármacos que cubren unha necesidade médica urxente, como é o caso da actual pandemia.
https://twitter.com/EMA_News/status/1346793570334867457
Despois deste paso, a Comisión Europea supervisou todo o procedemento e consultou aos estados membros da Unión, que apoiaron o trámite preciso. Segundo expuxo a presidenta da Comisión, Ursula von der Leyen, a UE recibirá 160 millóns de doses da vacina de Moderna. Sumadas aos 300 millóns de Pfizer-BioNTech, poderanse administrar 460 millóns con estas dúas vacinas aprobadas, e agárdase que nas vindeiras semanas tamén se dea luz verde a outros proxectos, como o de Oxford-AstraZeneca.
https://twitter.com/ComisionEuropea/status/1346849349184192516
Como é a vacina de Moderna?
Do mesmo xeito que a de Pfizer-BioNTech, está baseada no ARN mensaxeiro (ARNm), unha técnica moi novidosa nas vacinas, que supuxo un grande investimento económico. A vacina de Moderna é quen de ‘ordenar’ ao noso corpo a fabricación de fragmentos do SARS-CoV-2 que o organismo humano utiliza para desenvolver a resposta inmunitaria contra a súa infección, sen a necesidade de introducir, como nas vacinas máis ‘tradicionais’, patóxenos atenuados.
Así, este ARNm inclúe as instrucións para que o noso ADN fabrique a coñecida proteína S (‘spike’ ou espícula) do SARS-COV-2, que o coronavirus utiliza para entrar nas células. Cando unha persoa recibe a inxección, as súas células len as instrucións do ARNm e producen esta proteína. Ao mesmo tempo, a detección desta proteína provoca que o organismo reaccione, recoñecendo o posible patóxeno, producindo anticorpos e activando as células T (glóbulos brancos) para atacar a proteína e destruíla.
Deste xeito, se posteriormente, unha vez recibidas as dúas doses e adquirida a inmunidade, a persoa vacinada entra en contacto co SARS-CoV-2, o organismo reaccionará fronte a el.
Como de efectiva é a vacina de Moderna?
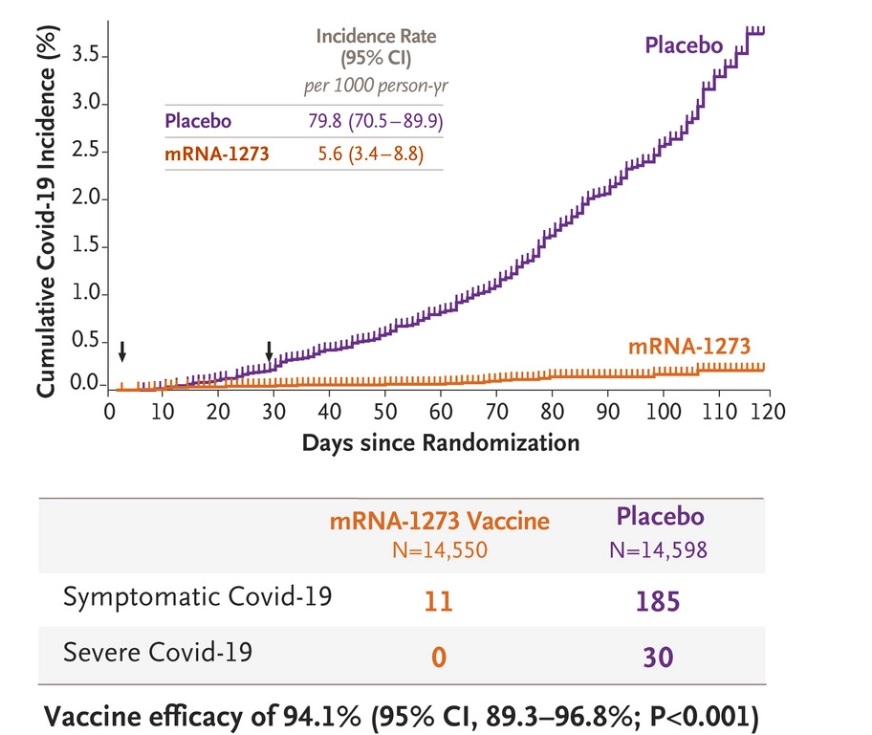
Os ensaios clínicos realizados ata o momento en 30.000 persoas constataron unha redución do 94,1% dos casos sintomáticos de Covid-19 no grupo que recibiu a vacina. Só 11 das 14134 persoas vacinadas desenvolveron a enfermidade, mentres que no grupo de control, que recibiu placebo, 185 das 14073 persoas desenvoveron síntomas da Covid-19. Ademais, segundo os datos que a empresa remitiu á EMA, e que foron analizados por este organismo, a vacina de Moderna tiña tamén un 90,9% de eficacia nas persoas con factores de risco, como enfermidades crónicas de pulmón ou corazón, obesidade, problemas hepáticos, diabetes ou VIH.
Conservación, doses, etc.
Unha das claves da primeira etapa de vacinación co antídoto de Pfizer-BioNTech está a ser o de manter a cadea de frío precisa para non degradar o medicamento. A vacina de Moderna permanece estable durante varios meses a -20ºC, e pode resistir 30 días nun frigorífico ‘normal’, entre 2 e 8ºC, o que supón un avance respecto á outra inmunización aprobada. Tamén require de dúas doses, que deberán ser administradas cun espazo de arredor de 28 días entre a primeira e a segunda.
Efectos adversos, na transmisión, en nenos…?
Nin a vacina de Moderna nin a de Pfizer-BioNTech puideron constatar, por agora, que a inmunización free a transmisión dunha persoa a outra. Estanse a facer investigacións continuas para avaliar esta opción, e outros proxectos, como o de Oxford-AstraZeneca, si parecen constatar que o feito de recibir a vacina reduce tamén o risco de que unha persoa transmita o virus.
No referente aos efectos adversos, como calquera outro produto sanitario, poden xurdir reaccións en persoas alérxicas. Unha de cada 10 persoas que participou nos ensaios clínicos tivo leves síntomas, como dor ou molestias na zona de inxección, cansazo, calafríos, febrícula ou dor muscular. Outros efectos adversos foron menos comúns (menos de 1 de cada 100), como comechón na zona da picada. Menos de 1 de cada 1000 persoas epxerimentaron parálise temporal na cara.
No caso da vacina de Moderna, a EMA recomenda que non reciban a vacina as persoas alérxicas a algúns dos compoñentes do fármaco, que se poden consultar na información de produto (PDF). Nos ensaios clínicos observáronse moi poucos casos de anafilaxe grave. De todas formas, nas persoas nas que se observan reaccións graves despois de recibir a primeira dose desaconsellarase que se administre a segunda.
No caso de persoas inmunocomprometidas, os datos son limitados, pero por agora non hai preocupacións sobre a seguridade da vacina de Moderna. Toda vez que estas persoas están en risco de que a infección complique a súa evolución, recoméndase a súa vacinación. Os datos tamén son limitados no caso das mulleres embarazadas ou lactantes, e aínda que non se observaron problemas, recoméndase que se considere cos profesionais médicos a decisión de vacinarse.
O ensaio clínico da vacina de Moderna implicou a persoas maiores de 18 anos, polo que non se recomenda por agora o seu uso en menores. De todas formas, a EMA acordou coa compañía desenvolver un novo ensaio para estudar este aspecto. Así, tanto Moderna como Pfizer-BioNTech seguen adiante con análises, en coordinación coas distintas axencias, para optimizar os seus antídotos.